NFCR
4月7日,《自然》在线发表了美国范德比尔特大学Kimryn Rathmell研究团队的研究成果。这篇文章的标题是“肿瘤微环境中细胞程序化的营养分配”。 ) 最新的研究结果可能会改变之前认为肿瘤细胞在肿瘤微环境中具有更高水平的葡萄糖摄取的看法。
研究认为,肿瘤细胞以前并没有被认为是高糖代谢的罪魁祸首,但被称为巨噬细胞的免疫细胞具有高糖代谢水平。
这一发现颠覆了过去一个世纪肿瘤微环境中代谢竞争的普遍看法,有助于开发新的抗癌疗法和新的癌症诊断和检测成像策略。

Reinfeld, B.I., Madden, M.Z., Wolf, M.M.等。肿瘤微环境中细胞程序化的营养分配。自然 (2021)。 />
癌症代谢领域在过去的 20 年中确实出现了爆炸式增长,但根据 Otto Warburg 在 1922 年发表的这一观察结果,癌细胞可以以非常高的速度消耗葡萄糖。
在正常细胞中,葡萄糖会保持平衡状态。在缺氧状态下,葡萄糖会转化为丙酮酸,再转化为乳酸。当含氧量正常时,丙酮酸会进入三羧酸循环(TCA)循环。 .即使在有氧条件下,肿瘤细胞也不使用线粒体氧化磷酸化能力,而是使用有氧糖酵解,即 Warburg 效应。
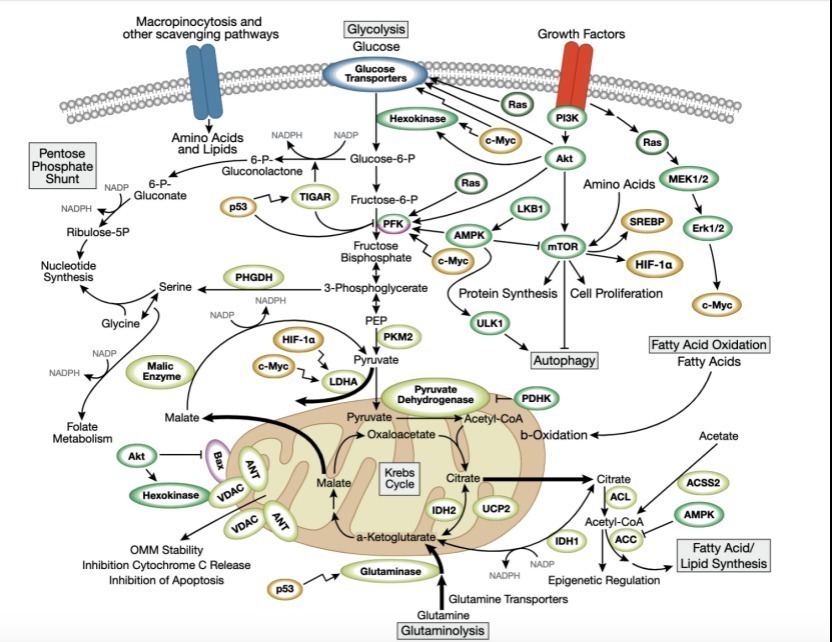
Warburg 效应路径,2021 年?细胞信号技术
Warburg 效应代表了肿瘤细胞利用葡萄糖的方式从氧化磷酸化到糖酵解的转变,被认为是肿瘤的一个主要特征。瓦尔堡效应的内部机制非常复杂。虽然相应的监管机制近年来已经提出并得到证实,但仍有许多问题亟待解决。因此,研究Warburg效应的关键调控点将有助于揭示肿瘤细胞的转移。该机制为肿瘤的靶向治疗提供了良好的方向和策略。
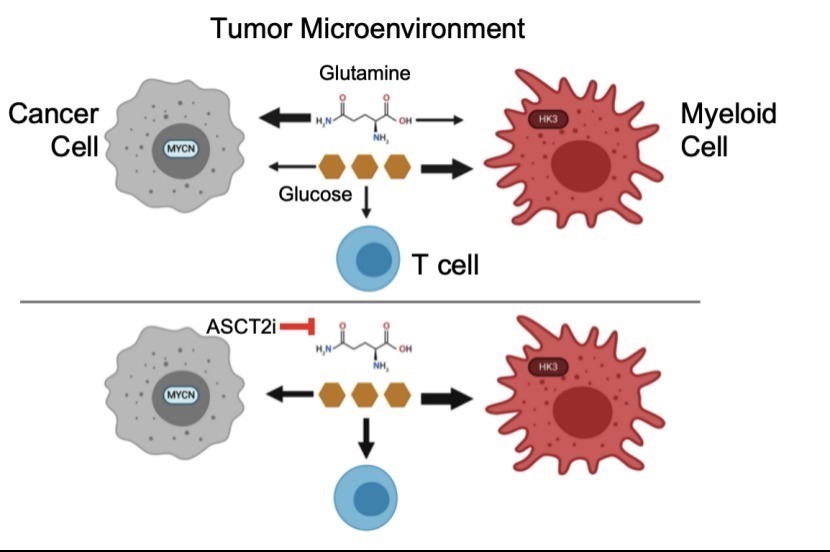
肿瘤微环境
肿瘤浸润免疫细胞也依赖葡萄糖,肿瘤微环境(TME)中受损的免疫细胞代谢有助于肿瘤细胞逃逸。然而,目前尚不清楚 TME 中免疫细胞的代谢是否因内源性细胞程序或与癌细胞竞争有限的营养而失调。
该研究使用 PET 示踪剂来定位和测量 TME 中特定细胞亚群对葡萄糖和谷氨酰胺的访问和摄取。在肿瘤微环境中,可以通过FDG(18F-氟脱氧葡萄糖)正电子发射断层扫描技术监测葡萄糖摄取,监测肿瘤细胞的反应和治疗。
研究团队使用两种不同的 PET 示踪剂分别跟踪葡萄糖和谷氨酰胺。在一系列肿瘤细胞模型中发现了髓系免疫细胞,包括结直肠癌、肾癌和乳腺癌细胞。 (主要是巨噬细胞)对葡萄糖的摄取量最高,其次是 T 细胞和肿瘤细胞。肿瘤细胞对谷氨酰胺的摄取量最高。研究小组认为,这是一种普遍现象,在多种肿瘤类型中也存在。
该研究检测了人肾癌细胞和小鼠皮下 MC38 肿瘤软组织间质液中的营养物质,发现肿瘤微环境中葡萄糖、谷氨酰胺和乳酸的浓度与健康肾组织或血浆中的水平相匹配。相似的。然而,正常细胞和肿瘤细胞之间葡萄糖和谷氨酰胺的代谢水平存在显着差异。
研究人员还通过CD45+标记将肿瘤微环境中的细胞分为CD45-肿瘤细胞和CD45+免疫细胞,发现免疫细胞可以消耗更多的葡萄糖。免疫组化和FDG实验结果表明CD45+免疫细胞的空间分布没有显着差异。这表明细胞营养摄取的差异并不是由免疫细胞的肿瘤微环境中存在特定空间引起的。
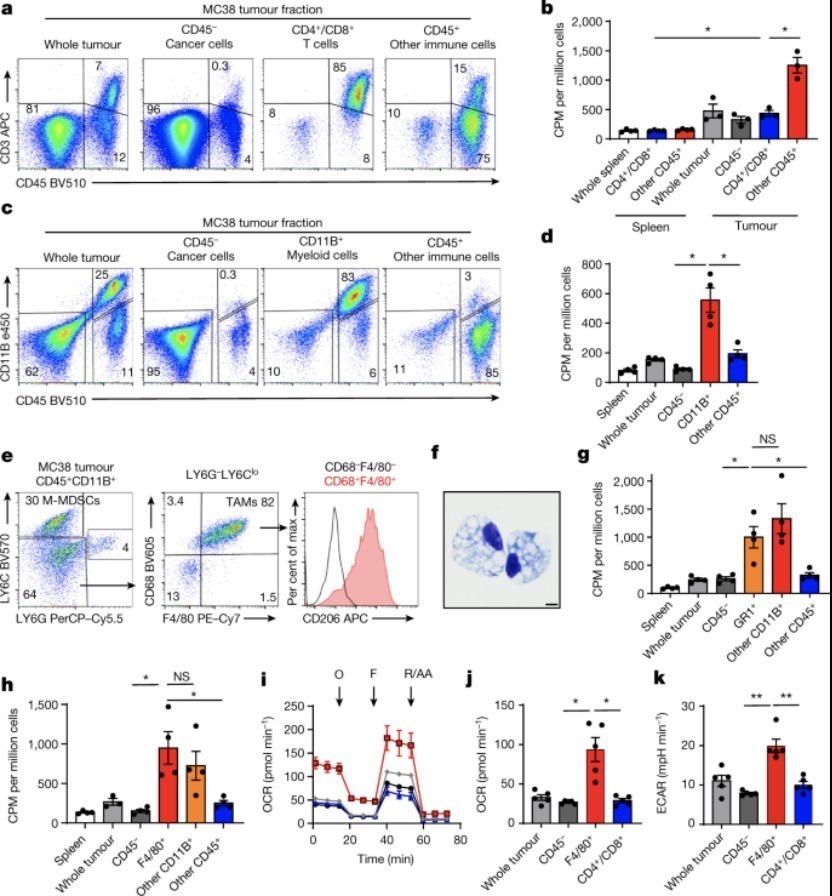
TME骨髓细胞比癌细胞吸收更多的葡萄糖
通过对 CD45+ 的进一步流式细胞术分析,与其他 CD45+ 细胞相比,分离的 CD11B+ 标记的骨髓细胞具有最高水平的葡萄糖摄取。此外,CD11B+标记的骨髓细胞在B细胞和T细胞缺陷小鼠中仍表现出高葡萄糖摄取能力,表明骨髓细胞的高葡萄糖摄取效率并未通过适应性免疫。
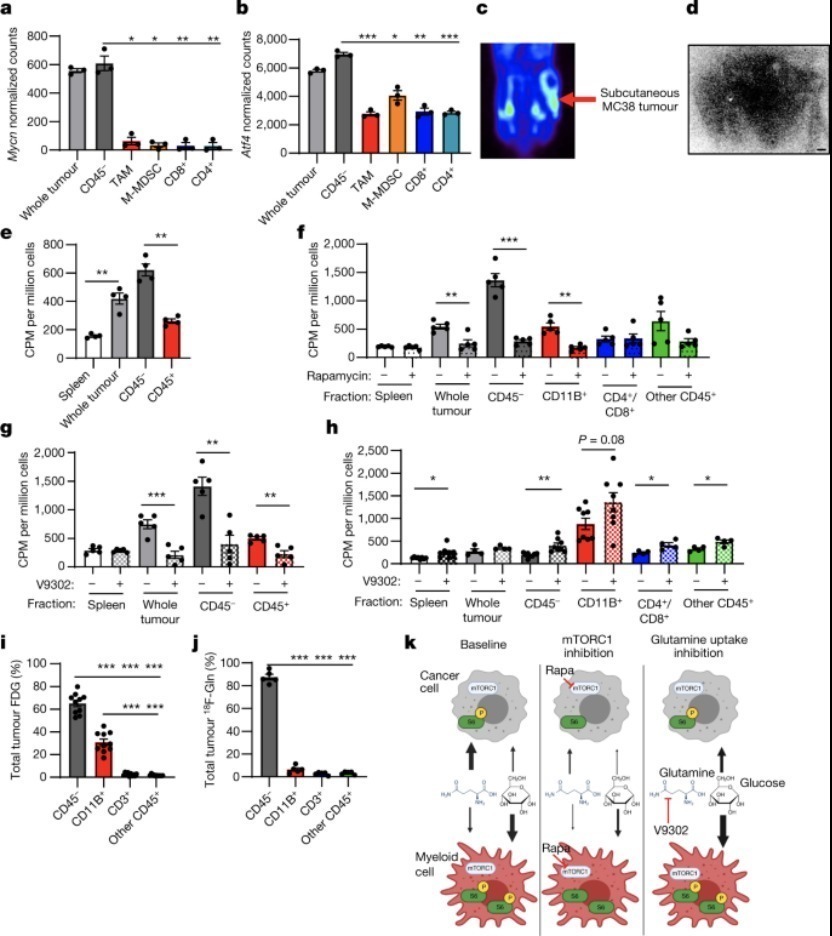
mTORC1 支持 TME 中的葡萄糖摄取和代谢
文章指出,此前的研究表明,哺乳动物体内的mTORC1支持身体的合成代谢和营养吸收。 mTOR(哺乳动物雷帕霉素靶蛋白)是雷帕霉素受体蛋白,主要在哺乳动物中进行研究。与人透明细胞肾细胞癌和小鼠 MC38 和 CT26 肿瘤中的其他肿瘤细胞亚群相比,mTORC1 通路在肿瘤骨髓细胞中具有更高水平的磷酸化核糖体蛋白 (pS6) 活性。
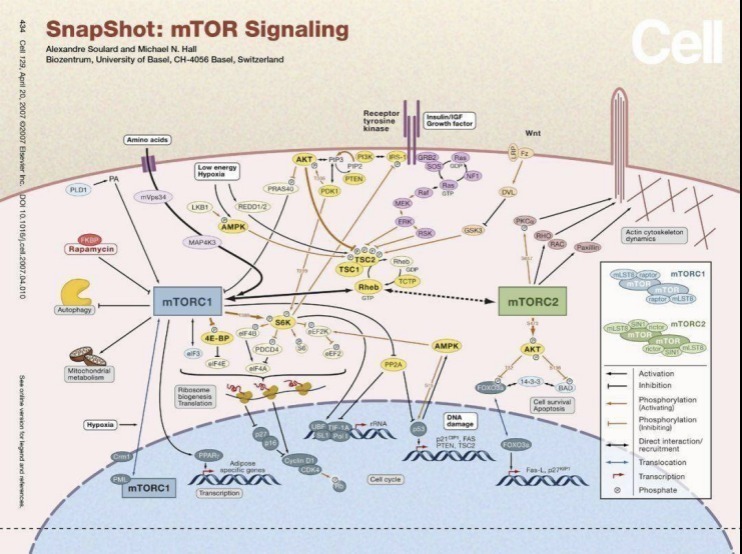
mTORC1 信号通路,CELL
因此,研究人员进一步研究了mTORC1信号通路是否参与了肿瘤微环境中葡萄糖的摄取。用雷帕霉素治疗小鼠MC38肿瘤后,测试了肿瘤细胞亚群吸收营养的能力。雷帕霉素是一种经典的 mTOR 抑制剂,可以同时抑制该通路中的两大块 mTORC1 和 mTORC2 的活性。结果表明,雷帕霉素治疗会下调 pS6 水平和 T 细胞浸润性疾病。这表明 mTORC1 信号通路参与了肿瘤微环境的代谢。
上一篇:肿瘤术后又遇皮损!北京中医医院多科室联合帮
下一篇:没有了








