
《肿瘤》

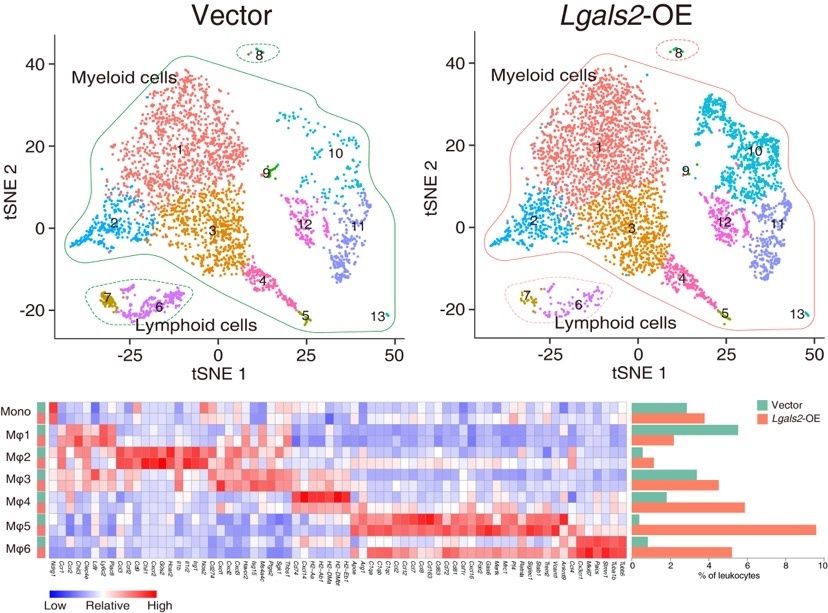
通过进一步的表型研究和机制探究,研究团队借助动物模型、单细胞测序技术、RNA测序技术、细胞共培养技术等,研究人员发现关键分子LGALS2主要通过调控集落刺激因子1及其受体轴(CSF1/CSF1R),招募更多的肿瘤相关巨噬细胞浸润到肿瘤微环境中,同时促进这些肿瘤相关巨噬细胞向具有抗炎及促肿瘤作用的M2型方向极化,从而增加了肿瘤微环境中的免疫抑制现象。因此,靶向LGALS2的治疗有望成为三阴性乳腺癌新的免疫治疗策略(图二)。

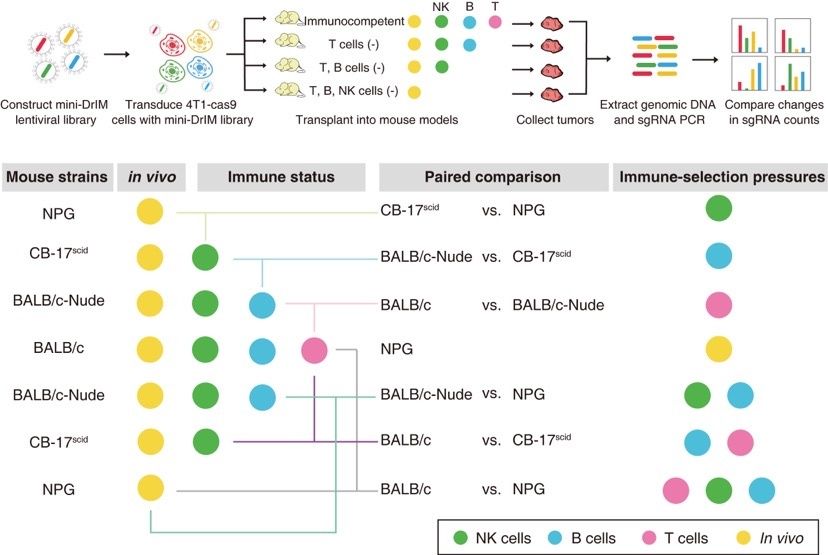
能否有效筛选并甄别肿瘤免疫基因,为肿瘤精准治疗奠定基础?为此,复旦大学附属肿瘤医院研究团队以三阴性乳腺癌为切入点,对2796个疾病相关免疫基因进行CRISPR/Cas9基因编辑,构建了“Dr. Immune”(免疫医生)文库。通过将导入文库的三阴性乳腺癌细胞分别种植到免疫力完整和免疫力重度缺陷的小鼠中,监测和分析肿瘤生长过程中富集或丢失的细胞。批量性观察在“肿瘤-免疫”的交互状态下,这些基因在小鼠体内究竟是参与免疫监视,还是免疫逃逸。
图一:“Dr. Immune”(免疫医生)筛选模式图
关键分子LGALS2打破三阴性乳腺癌免疫治疗“瓶颈”
基于第一轮“免疫医生”的筛选,研究团队进一步升级,定制开发出更为精细的 “mini-Dr. Immune”(迷你免疫医生),放到设计更精妙的多维免疫状态下开展二轮筛选。通过一轮轮筛选的抽丝剥茧,发现同一基因在不同免疫状态下,对抗肿瘤的协同/拮抗作用可能是不同的,有的甚至截然相反。这个发现很好演绎了同样的免疫治疗在部分患者身上有效,但在部分患者身上无效的情况,这一情况很可能与患者本身的免疫状态有关(图一)。
东方网通讯员胡欣、王广兆6月30日报道:作为一种治疗肿瘤的新方法,免疫治疗近年来飞速发展,已经应用于多种肿瘤的临床治疗,并取得良好效果。然而,对于有“最毒乳腺癌”之称的三阴性乳腺癌,以靶向PD-1/ PD-L1为首的免疫治疗却依然存在受益人群有限、缺少疗效预测指标等局限性,这也成为全球医学界亟需破解的难题之一。
6月30日,从复旦大学附属肿瘤医院传来消息,该院乳腺外科主任兼复旦大学肿瘤研究所所长邵志敏教授、精准肿瘤中心胡欣研究员、乳腺外科狄根红教授领衔的团队,通过构建“免疫医生”文库,结合团队三阴性乳腺癌多组学研究,首次成功锁定基因“半乳糖结合凝集素2”是三阴性乳腺癌介导免疫逃逸的“帮凶”,并且有望成为三阴性乳腺癌免疫治疗新靶点,为三阴性乳腺癌的免疫治疗提供了新的方向。该项成果同日于国际权威期刊《科学·进展》(Science Advances)在线发表,影响因子14.95分。
随后,研究团队进一步开展动物体内实验,发现无论是靶向LGALS2所调控的CSF1/CSF1R轴的药物,还是直接靶向LGALS2的中和性抗体药,都取得了显著的疗效,肿瘤的生长受到明显抑制,三阴性乳腺癌免疫微环境中的免疫抑制现象显著逆转。这些结果均提示,LGALS2作为三阴性乳腺癌潜在的免疫治疗新靶点,有望突破目前三阴性乳腺癌免疫治疗的瓶颈,打开免疫治疗的新局面,为三阴性乳腺癌患者延长生存提供崭新的机会和可能。
图二:LGALS2通过招募肿瘤相关巨噬细胞,并促进其向M2方向极化,促进免疫逃逸
“免疫医生”筛选“最毒乳腺癌”免疫逃逸“帮凶”
在三阴性乳腺癌中是否是有关键分子,总是能“帮助”肿瘤细胞伪装,逃避免疫系统中各路免疫细胞的追杀呢?根据“免疫医生”的筛选结果,并基于复旦肿瘤乳腺团队邵志敏教授、江一舟教授等已开展的三阴性乳腺癌多组学研究,研究团队成功锁定半乳糖结合凝集素2(Lectin galactose-binding soluble 2, LGALS2)为三阴性乳腺癌介导免疫逃逸的关键分子。
人的身体里每天都有肿瘤细胞产生,但与生俱来的免疫系统会形成一种防御和保护机制,这个系统就像体内的警察一样,能识别对身体不利的细胞,随时进行摧毁和清除。如果免疫功能异常,机体就不能识别恶性细胞,则容易形成肿瘤。
【来源:东方网】
上一篇:五华县人民医院外科部李震东教授为肝癌复发患
下一篇:没有了